

何川
1Nature:m6A通过(guò)YTHDF 1促进海马依赖(lài)性学习和记忆

N6-甲基腺苷(m6A)是哺乳动物信使RNA上最普遍的内部RNA修饰,通过m6A特异性结合蛋白(bái)调(diào)控修饰转录的目的和功能。在神经系统中,m6A数量丰富,功能多样(yàng)。在之前的研究中人们得知(zhī),m6A标记不同生理过程中协调降解的mRNAs组,但是(shì),在体(tǐ)内m 6A和mRNA翻(fān)译的相关(guān)性(xìng)仍然是未知的。
本文中(zhōng),研究人员发现,通(tōng)过结合蛋白YTHDF 1,m6A促进成年小鼠海马体神(shén)经元刺激反应的转录的(de)蛋(dàn)白(bái)翻译,从而(ér)促(cù)进学(xué)习和记忆。敲除(chú)Ythdf 1基(jī)因的小(xiǎo)鼠显示学习和记忆缺陷以及海马突触传递受损。YTHDF 1在成年Ythdf 1-敲除小鼠(shǔ)海马体(tǐ)中的再表达,可以(yǐ)修复(fù)行为和突触缺陷,而海(hǎi)马体(tǐ)上(shàng)特异性精确敲除Ythdf 1或METTL 3(其(qí)编(biān)码了m6A甲基转移(yí)酶复合物中(zhōng)的催(cuī)化组分)则重现为海马体缺乏症。海马体上mRNAs的YTHDF 1结合(hé)位点和(hé)m6A 结(jié)合位点确定了关(guān)键的神经元基因(yīn)。新生(shēng)蛋白标记和海(hǎi)马体神经元(yuán)系绳(shéng)报告试验表明,YTHDF 1以神经(jīng)元刺激依赖的方式促进(jìn)蛋白质合成。总之(zhī),YTHDF 1有助于(yú)翻译m6A-甲基化神经元mRNAs对神经元刺(cì)激的(de)反应(yīng),这(zhè)一过程有(yǒu)助于学习和记忆。
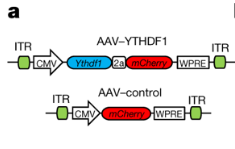
高表达YTHDF1(AAV-YTHDF 1)和(hé)对照(AAV-对照)的AAV结构示意图(tú)。
研究(jiū)证明,YTHDF 1的缺失损害了海马体突触的(de)基础传递(dì)和LTP。YTHDF 1的存在可以(yǐ)加速新的蛋白质合成(chéng),这是突触可塑(sù)性和记忆形成的长期变(biàn)化所必需的;Ythdf 1-KO小(xiǎo)鼠,刺激依赖的蛋白(bái)质合成减弱,导致(zhì)突触强化效率较低,达到(dào)记忆(yì)形成(chéng)阈值的可能性较低。m6A对翻译的促进作用可能是通过刺激诱(yòu)导,如(rú)文中对(duì)YTHDF 1的(de)作用,这(zhè)可能代表RNA甲基化依赖的(de)翻译(yì)调节的(de)一(yī)个重要方面。
原文链接:
https://www.nature.com/articles/s41586-018-0666-1
2Cell Research:A dynamic N6-methyladenosinemethylome regulates intrinsic and acquired resistance to tyrosine kinaseinhibitors

白血病是一种侵袭性恶性肿瘤,通常与激活(huó)受体酪氨酸(suān)激酶(RTKs)突变(biàn)有(yǒu)关,包括BCR / ABL,KIT和FLT3等。许多针(zhēn)对这些(xiē)突(tū)变的酪氨酸激酶抑(yì)制剂(TKIs)已进入(rù)临床,但迅速(sù)获(huò)得对(duì)TKIs的(de)抵抗是成功(gōng)治疗(liáo)白血病的主要障碍(ài)。最常被引用的机制是获得(dé)性药物抗(kàng)性突变(biàn),其损害药物结合或(huò)绕(rào)过抑制(zhì)的RTK信号传导。然而,这(zhè)不足以揭示药(yào)物暴露后(hòu)TKI耐药性的出现相对迅(xùn)速的情况。在(zài)“药物假期”之后,抗性(xìng)表型是可逆的(de)。许多具有抗性的患者也仅(jǐn)表达(dá)天然激酶(例如,BCR / ABL)或已经激活平(píng)行途径,涉及(jí)癌基因的过度简化(例(lì)如,BCL-2,BCL-6,AXL和MET)。
事实(shí)上,最近的研究结果已(yǐ)经将获(huò)得性TKI耐药性与肿瘤内的细胞异质性和(hé)表观基因组构型的动态变异联(lián)系起来。据推测,异质性肿(zhǒng)瘤细(xì)胞群中不同的表观遗(yí)传模式可以在细胞命运(yùn)决定基因的表达中(zhōng)产生多样性。通过药(yào)物选择可以迅速发展。然而,TKI抗性中关键表观遗传事件的(de)描述远未完成。
N6-甲基腺苷(m6A)是哺乳动物(wù)mRNA最常见的上皮转录组修饰.14,15,16它由甲基转移酶复合(hé)物(如METTL3-METTL14)安装,可被去甲基化(huà)酶清除(如FTO和ALKBH5)。虽然任何特定(dìng)m6A残基(jī)的确切作用尚不(bú)清楚,但21个丰富的证据支持m6A甲基化,一般来说,严格调节mRNA稳定性,剪接(jiē)和/或蛋白质翻译,从(cóng)而影响基因表达(dá)。一致地,沉默m6A甲(jiǎ)基转移酶(méi)(例(lì)如,IME4,METTL3的酵母(mǔ)直向同(tóng)源物)或FTO的敲低改变(biàn)m6A丰度,重新建模基因表(biǎo)达谱和(hé)/或转录(lù)物(wù)的(de)可变剪(jiǎn)接模式。
尽管最近关(guān)于角色的工作m6A在各种生(shēng)物学过程中的作用(yòng),m6A甲基化是(shì)否以及如何调节TKI选择下的细胞(bāo)命运决定仍然未知。我们假设,暴(bào)露(lù)于(yú)TKI后(hòu),m6A甲基(jī)化的可逆性质使得(dé)携带(dài)m6A位点的(de)一(yī)组增殖(zhí)/抗凋亡(wáng)癌基因上(shàng)调,从而帮助细(xì)胞亚群逃避TKI介导(dǎo)的杀伤。为(wéi)了测试这一点,我们模拟并表(biǎo)征了不同白血病(bìng)模型中的TKI抗性,并直接在白血病(bìng)细胞的转录组中定位m6A。我们的研究结果表明,内在和(hé)诱导(dǎo)型FTO-m6A轴作为表(biǎo)征白血(xuè)病细胞异质性(xìng)的新标记,以及(jí)白(bái)血病细胞产生TKI抗性表型的广泛(fàn)防(fáng)御机制。我们的发现确(què)定了针对FTO-m6A轴预防/根除获得性TKI耐(nài)药性的可行性。
研究(jiū)人员的(de)研(yán)究结果显示在酪氨酸激酶抑制剂(TKI)治疗期间开发抗(kàng)性表型取决于白血(xuè)病(bìng)细胞中(zhōng)FTO过(guò)表(biǎo)达导致(zhì)的m6A减少。这种失调的FTO-m6A轴预先存在于幼稚细胞群中,这些细胞群具(jù)有遗传同质性,并且(qiě)响应TKI处理是(shì)可诱导/可逆的。具有mRNAm6A低甲(jiǎ)基化和(hé)FTO上调的细胞在小鼠中表现(xiàn)出更高的TKI耐受性和更高的(de)生长速率(lǜ)。通(tōng)过FTO失活的m6A甲基(jī)化(huà)的遗(yí)传或药理学恢复使得对(duì)TKI敏感的抗性细胞。
从机制上讲,FTO依赖性(xìng)m6A去甲基化增强了携带m6A的(de)增殖/存活转录(lù)物(wù)的(de)mRNA稳定(dìng)性,并随后导致蛋白质合成增加。我们的(de)研究结果确定了m6A甲基化在调节细胞命运决定(dìng)中的新(xīn)功(gōng)能,并证明动态m6A甲基化组是可逆TKI耐受状态的额外表观遗传驱(qū)动因子,为癌症中(zhōng)的耐药性提(tí)供了机制典型范(fàn)例。
3Cell:m6A可以控制哺乳动物的皮质神经元的发生

由(yóu)Mett13 / Mett14甲基转移酶复(fù)合物催化产生的N6-甲基腺(xiàn)苷(m6A)是最普(pǔ)遍的(de)mRNA内部(bù)修饰。 m6A是否调节哺乳动物的大脑发育是未(wèi)知的。在这里,我们显示胚胎小(xiǎo)鼠脑(nǎo)中(zhōng)Mettl14敲除下,m6A缺失(shī),延长了神经胶(jiāo)质细胞(bāo)的细胞周期,并(bìng)将皮(pí)质神(shén)经(jīng)发(fā)生(shēng)延伸到出生后阶段;通过Mettl3敲除,也(yě)得到了类似(sì)的(de)现象。胚(pēi)胎小鼠皮层的m6A测(cè)序显示,m6A主要富集在转录(lù)因(yīn)子(zǐ),神经发生,细胞周期和神经元分化的mRNA中,m6A标记(jì)促进其衰老。进一步(bù)的分析发现皮质神经干细胞中以前未被认可的转(zhuǎn)录模式中,m6A信号也调(diào)节前脑组织中的(de)人(rén)皮质(zhì)神经(jīng)发(fā)生。小鼠(shǔ)与人类(lèi)皮质神(shén)经发生之(zhī)间的(de)m6A-mRNA全基(jī)因组的比(bǐ)较(jiào),揭示了人(rén)特异(yì)性m6A标记的(de)转录本与脑障碍风险(xiǎn)基因相(xiàng)关(guān)。
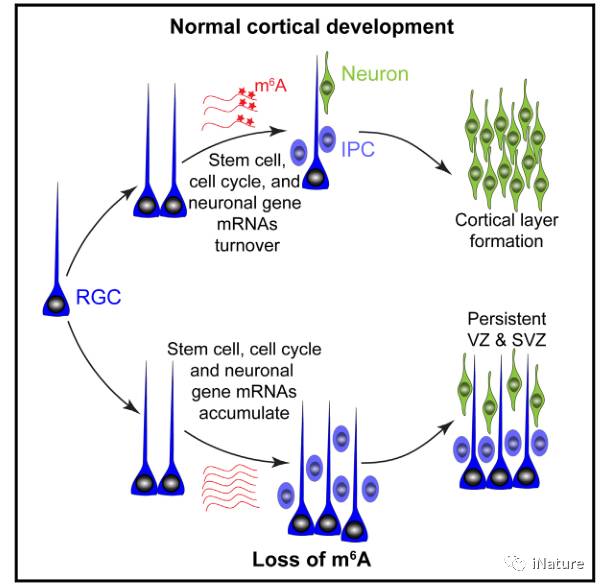
亮点(diǎn)
m 6 A缺失,导致(zhì)皮质(zhì)神经原始细胞的细胞周期(qī)延(yán)长;
经过比(bǐ)较小鼠及(jí)人(rén)类的m 6 A图谱,呈现(xiàn)出(chū)保守(shǒu)及独特性(xìng);
m 6 A促进标记的神经发生相关的转(zhuǎn)录本(běn)被延迟降解;
转录本(běn)的提前印(yìn)记对于神经元的发生是必需的。
4Molecular Cell :FTO在细胞核(hé)和细胞质中介导的(de)差异m6A,m6Am和m1A去甲基化

已经提出脂肪(fáng)量和肥胖相关蛋白(FTO)通过全基(jī)因(yīn)组(zǔ)关联研究(GWAS)与(yǔ)人类(lèi)肥胖相关联。已(yǐ)显示(shì)FTO的遗传变异与食物摄入增加有关,而FTO中的功能丧失突变导致严重(chóng)的生长迟缓和CNS缺陷。
由于这(zhè)些有趣的表(biǎo)型,已经广泛致(zhì)力于鉴定(dìng)底物和理解FTO的生(shēng)物学(xué)功能。FTO被鉴定为第一种RNA去甲基化酶,其在(zài)体外和细胞中(zhōng)催化mRNA中(zhōng)N6-甲基腺苷(m6A)甲基化的(de)逆(nì)转。 m6A是哺乳(rǔ)动物mRNA中(zhōng)最(zuì)丰富的内部(bù)修饰。已(yǐ)知m6Am的m6A部分是FTO的体外(wài)底物,最近(jìn)的研究表(biǎo)明m6Am通过阻止DCP2介导的脱帽和microRNA介导的mRNA降(jiàng)解来稳定mRNA。然而(ér),FTO去除m6Am的功能(néng)相关(guān)性(xìng)尚未得到充分探索。
在该项研究组中,何川(chuān)研究组证实(shí)FTO可(kě)以从(cóng)纯化的多腺苷酸化RNA中有效地(dì)去(qù)甲基化m6A和m6Am。何川研究(jiū)组发现细胞核和(hé)细胞质中的FTO定位在细胞类型之间变化,并且FTO在细胞核和细胞质中具有(yǒu)不(bú)同的底(dǐ)物库(kù)。何(hé)川研究组进一步(bù)鉴定了FTO的其他RNA底(dǐ)物,包(bāo)括tRNA中(zhōng)的(de)N1-甲基腺苷(m1A),U6 RNA中(zhōng)的m6A,以及小核RNA(snRNA)中的内(nèi)部和帽m6Am。该研究提供了迄今为止FTO介导(dǎo)的RNA去(qù)甲基化的最全面(miàn)的景观。它揭示了由FTO介导的核与(yǔ)细胞质去甲(jiǎ)基化所(suǒ)赋(fù)予的先前未被认(rèn)可的空间调节,其对靶RNA发(fā)挥不同的作用。
5Nature cell biology:m6A mRNA甲基化是子宫(gōng)内膜癌的致癌机制

N6-甲基(jī)腺苷(gān)(m6A)是(shì)人类最普遍的信使RNA修饰形式。这(zhè)种修改是(shì)可逆(nì)的,其(qí)生物(wù)学效应主要是通(tōng)过(guò)“写入”、“橡皮”和“读取(qǔ)”蛋白(bái)来介导的。所谓的(de)“写入”复合物,核心部分(fèn)为METTL3–METTL14 m6A甲基转移酶(méi),还包(bāo)括其他调控因子亚单元,作用是(shì)催化m6mRNA甲基化。至少有两种(zhǒng)橡皮擦酶FTO和ALKBH 5介导(dǎo)了(le)甲基化的逆反应。m6甲基化的转录被读(dú)取器(qì)蛋白质锁(suǒ)识别,该蛋白可以调节(jiē)mRNA前处理(lǐ)、翻译和退化(huà)。在哺乳(rǔ)动物中,m6A依(yī)赖(lài)的mRNA调(diào)节是(shì)必(bì)不可少的(de)。m6A甲基化的缺陷影响很多的生物过程。特别的是,m6A mRNA甲基化通(tōng)过(guò)影(yǐng)响(xiǎng)细胞分化过(guò)程中mRNA的转换而调节干细胞的自我更新和分化,并在胚胎发育过程中(zhōng)对(duì)转录组的转换起重要作(zuò)用。与这些作用一致(zhì),m6A mRNA甲基(jī)化是一种影响多种癌(ái)症(zhèng)发(fā)生(shēng)和发展的途径(jìng)。
m6mRNA甲基化对干细胞和(hé)癌细胞生长和增殖有着(zhe)重要影响。不过,m6A甲(jiǎ)基化如(rú)何影响细胞生长,哪些基础途径和机制介导(dǎo)这些(xiē)变化仍未完全阐明。本(běn)文研(yán)究子宫(gōng)内膜癌(ái)中的(de)这个问题(tí),其中(zhōng)测序研究发现了m6A甲基转移酶亚基METTL 14的频繁突变(biàn)。研究(jiū)人(rén)员发现与对应的正常子宫内膜相比,约(yuē)有70%的子宫内膜肿瘤细胞中m6A甲基化有减少的趋势。这些减少的m6A甲基化可能是由(yóu)METTL 14的突变或降低METTL 3甲基转(zhuǎn)移酶的表达。通过METTL 14突变或METTL 3下调,降低m6A mRNA在子(zǐ)宫内膜癌(ái)细胞中的水平,可促进体外和活体(tǐ)细胞(bāo)增殖和致瘤(liú)性。子宫内膜癌(ái)患者肿瘤和细胞系的m6A -seq特(tè)征显示m6A mRNA甲基化可以通(tōng)过改变影响(xiǎng)AKT信(xìn)号通路(lù)的关键(jiàn)酶的表达来(lái)促进细胞增殖。抑(yì)制AKT活化可以逆转(zhuǎn)m6A甲基化减少引起的增殖增加。这些结果(guǒ)共同(tóng)表(biǎo)明了m6A mRNA甲(jiǎ)基化为子宫内膜癌的致癌(ái)机制,m6A甲(jiǎ)基化可以(yǐ)作为(wéi)AKT信号调节因子(zǐ)。
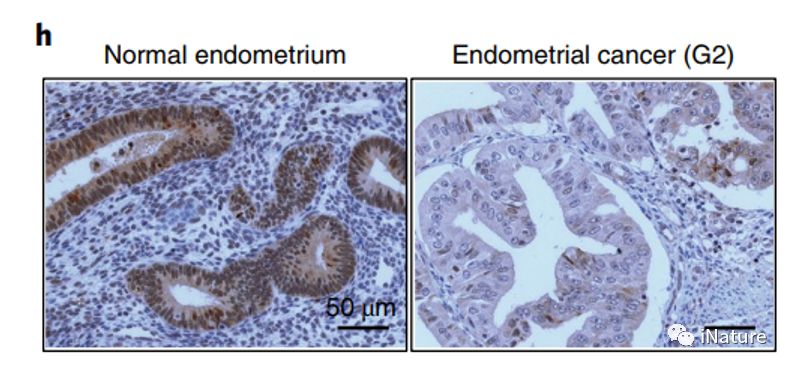 正常子宫内膜(mó)(左)和子(zǐ)宫内膜(mó)癌(右)
正常子宫内膜(mó)(左)和子(zǐ)宫内膜(mó)癌(右)
这些(xiē)发(fā)现可能适用于子宫内膜(mó)癌以外由AKT信号增(zēng)强所导致的(de)其他(tā)癌症。其他类型可(kě)以通(tōng)过AKT激活的肿瘤可以利用异常的RNA甲基化来获得生存(cún)和生长优势。事实(shí)上,也有其他研究观察到干细胞和(hé)癌细胞的增(zēng)殖(zhí)随(suí)着m6A甲基(jī)化的减少而增加。当这篇论文被(bèi)审(shěn)查(chá)时,据报道,m6A甲基化会影(yǐng)响(xiǎng)AML中AKT的活性,以及肾细胞癌30T细胞分化。虽然(rán)本(běn)文的结果表明m6A甲基化促进子(zǐ)宫内膜肿瘤发生,其他癌症也与METTL 3高表(biǎo)达和m6A甲基化增加有关,也可能涉及不同的机制。然而,我(wǒ)们的(de)结果表明,通过m6A甲基化调节(jiē)AKT的活(huó)性,可能是一种影响一系列(liè)其他生物过程(chéng)的一般生长控制机制,这将是未来(lái)探索(suǒ)的(de)一个新方(fāng)向。
6Molecular Cell:Zc3h13调节核RNA m6A甲基(jī)化和(hé)小鼠胚(pēi)胎干细胞(bāo)自我更新(xīn)

基因表达调控是(shì)生命(mìng)活动(dòng)的核心事件之一。RNA化(huà)学修饰是基因表达调控的重要手(shǒu)段。RNA m6A修饰广泛存(cún)在于病毒、细菌(jun1)、单细胞生物(wù)和(hé)酵母等多个物种中,是真核生物mRNA上发(fā)生(shēng)最为广(guǎng)泛的内部化学修饰。
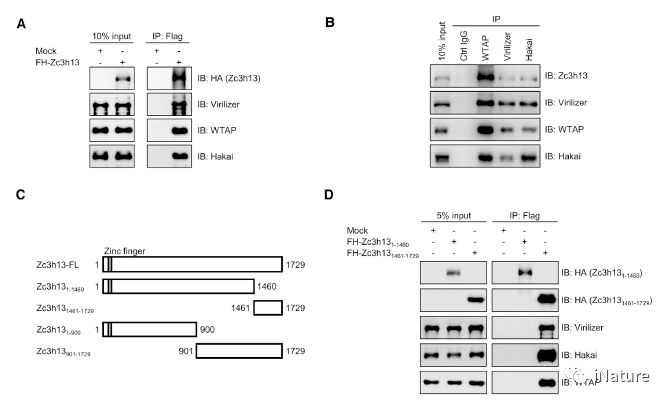
Zc3h13与WTAP,Virilizer和Hakai互作
RNA m6A修饰参与调节(jiē)mRNA稳定性、剪接加工、转(zhuǎn)运以及(jí)翻译等一系列mRNA加工(gōng)代谢过程,对mRNA的命运决定发挥重(chóng)要作用。越来越多的科学证据显示mRNA m6A修饰在细(xì)胞分化、生物个体发育及癌症(zhèng)疾病发生等一系(xì)列生命过程中具有重要作用,成为近(jìn)年来表观转录组学的研究热点之一。
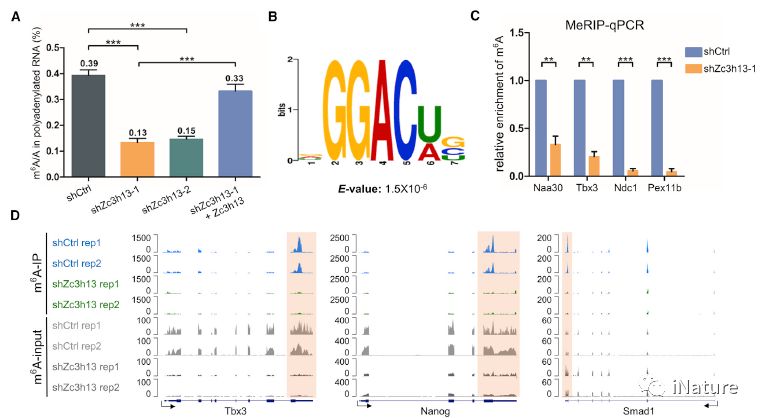
Zc3h13调节(jiē)mESCs中的mRNA m6A
哺(bǔ)乳动(dòng)物细胞中约25%的mRNA有m6A修饰,围(wéi)绕该修(xiū)饰的(de)甲基转(zhuǎn)移(yí)酶复合物、去(qù)甲(jiǎ)基转移酶和识(shí)别蛋白的研究较多(duō),但是参与该(gāi)修饰的调控蛋白以及(jí)该(gāi)修饰的位(wèi)点特异性调(diào)控机制依然不完全清(qīng)楚。在该(gāi)论文中,研究者报(bào)道(dào)了Zc3h13是一(yī)个(gè)调控RNA m6A修饰的(de)新成员。研究发现,在小鼠胚胎干细胞中抑制Zc3h13表达(dá)导致mRNA m6A水平(píng)显著(zhe)降低(dī),且这(zhè)些(xiē)下降的m6A主要(yào)发生在mRNA的(de)3’端非编(biān)码区(qū)域。

Zc3h13控制WTAP,Virilizer和Hakai的(de)核定位
此前(qián),有报道显(xiǎn)示Zc3h13存在(zài)于(yú)一个(gè)进化上(shàng)保守的复合物Zc3h13-WTAP-Virilizer-Hakai之中。研(yán)究者在探讨Zc3h13对m6A调控的分(fèn)子机制研究(jiū)中发现Zc3h13对m6A的调节是通过(guò)控制复合物成员(yuán)WTAP/Virilizer/Hakai的细胞定位而发(fā)生作用(yòng)的。抑制Zc3h13表达(dá)导(dǎo)致复合物成员WTAP、Virilizer及Hakai蛋白发生由细胞核向细胞质(zhì)的转移,同时伴随甲基转移酶Mettl3和Mettl14蛋白核内组分(fèn)的减少(shǎo),从而抑制m6A的形成。
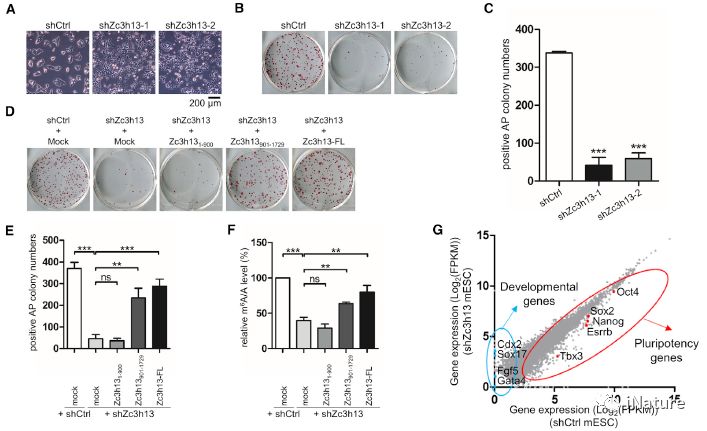
Zc3h13丧(sàng)失损害mESC自(zì)我(wǒ)更新
有意(yì)思的是,在细胞中敲低WTAP、Virilizer和Hakai,Zc3h13的核内定位并不受(shòu)影响,这(zhè)提示了Zc3h13在该复合物的(de)细胞定(dìng)位中具有独特(tè)的作用;同时(shí),也为揭示m6A 修饰的特异(yì)调(diào)控机制提供了(le)线索。此外,研究(jiū)者(zhě)还发现敲低Zc3h13会损害小(xiǎo)鼠胚胎干(gàn)细胞的自我更(gèng)新潜能并(bìng)促进细胞(bāo)的分化(huà),为(wéi)m6A途径调节小鼠胚(pēi)胎干细(xì)胞的多潜(qián)能性提供(gòng)了进一步(bù)的(de)证据和(hé)线(xiàn)索。

文章(zhāng)模(mó)型
复旦大学刁建波副研(yán)究员、施扬(yáng)教授、石雨(yǔ)江教授和芝加哥(gē)大学何川教授为论文的共(gòng)同通(tōng)讯作者(zhě)。复(fù)旦大学生物(wù)医(yī)学研究院博士(shì)研究生温菁、吕瑞途和博士后马红辉为论文的共同第一作(zuò)者。
7Cell Research:5-羟甲基胞嘧啶在循环无(wú)细胞DNA中的(de)特(tè)征是人(rén)类癌症的诊断(duàn)生物标志物

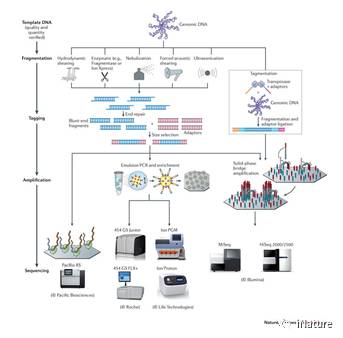
DNA修饰(shì)如5-甲基胞嘧啶(5mC)和(hé)5-羟(qiǎng)甲基胞嘧啶(5hmC)是已知影响哺乳动物基因表达(dá)的表观遗传学标记(jì)。鉴(jiàn)于(yú)它们在人类基因组中的广泛分布(bù)特(tè)性,与(yǔ)基因(yīn)表达(dá)密切相关和高度(dù)的化学稳定性,这些DNA表(biǎo)观遗传标(biāo)记可(kě)以作为癌症诊断的理想生物标志物。利用高度敏感和(hé)选择性的化学标记技术,何川等人在这(zhè)里收(shōu)集(jí)了最(zuì)近诊(zhěn)断患有(yǒu)结直肠癌,胃癌(ái),胰腺癌,肝癌或甲状腺癌的患者和来自90个(gè)健康个体的正常组织样品(pǐn),进(jìn)行对循(xún)环(huán)无细胞DNA(cfDNA)5hmC分析。
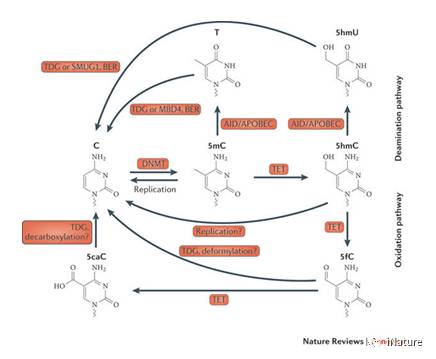
去甲基化过程(chéng)
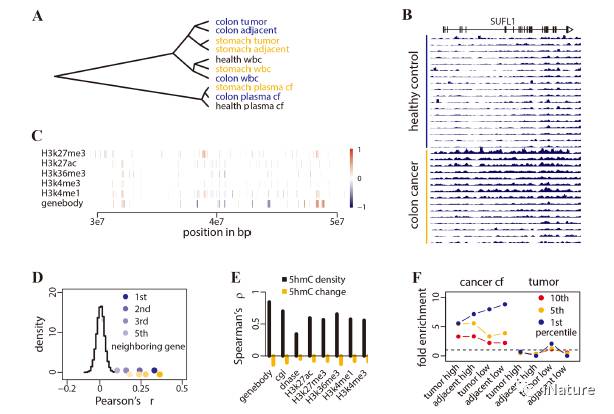
发现5hmC主要分(fèn)布在转录(lù)活性区域,与开放的染色(sè)质和活(huó)性组蛋白修饰相一致。在cfDNA中(zhōng)鉴定出可靠的癌症相关(guān)的5hmC标签,这是特定癌症类型的特征(zhēng)。基(jī)于5hmC的循环cfDNA生物标志物对结肠直肠癌和(hé)胃癌具有高(gāo)度预测(cè)性,优于常规生物(wù)标志(zhì)物,与来自(zì)组织活检(jiǎn)的5hmC生物标志物(wù)相当。因此,这种(zhǒng)新(xīn)的策略(luè)可以导致从血液(yè)样(yàng)本的分析(xī)中发(fā)展有效的,微创的癌症诊断和预后方法。
癌(ái)细胞释放DNA到血液
胞嘧啶甲基化(形成(chéng)5-甲基(jī)胞(bāo)嘧(mì)啶,5mC)是影(yǐng)响基因表达的公认的表观遗传学(xué)修饰【1,2】。 DNA的(de)5mC重构在哺(bǔ)乳动物(wù)发育和细胞分化以及癌症发生(shēng),进展和治疗反(fǎn)应过程中广泛使用【3,4】。哺乳动物基(jī)因组(zǔ)中的活性去甲基化是由将5mC修饰氧化为5-羟甲基胞嘧啶(dìng)(5hmC)【5,6】,以及进一步(bù)转化为5-甲酰基胞嘧(mì)啶(5fC)和5-羧基胞嘧啶(dìng)(5caC)的TET家族(zú)的双(shuāng)加氧酶完成(chéng)【7,8,9】。 “中间”5hmC不仅标志着活跃的去甲基化,而且还是一个相对稳定的(de)DNA标记,具有不同的表观(guān)遗传角色【2,10-15】。 5hmC在各种哺乳动物(wù)细(xì)胞和(hé)组织(zhī)中最(zuì)近的全基因组测序图谱支持(chí)其(qí)作为(wéi)基因表达(dá)的标记的作(zuò)用(yòng)【16-21】;它在增强(qiáng)子,gene body和(hé)启动(dòng)子富(fù)集,5hmC的变化与基因表达水平的变化(huà)相关【22,23】。
高通量(liàng)测序
来自循环血液中不同组织的无(wú)细胞DNA(cfDNA)的发现(xiàn)对临床具有革(gé)命性的潜在应用【24】。基于(yú)液体活检(jiǎn)的生物标志物和检测工具与现有的(de)诊断(duàn)和预后方(fāng)法相比(bǐ)具有显(xiǎn)著的优势,包括微创。因此(cǐ),他们具有成本(běn)效益的潜力,可以(yǐ)促进更高的患者依从性和(hé)临床便利性,从而实现动态监测【25】。
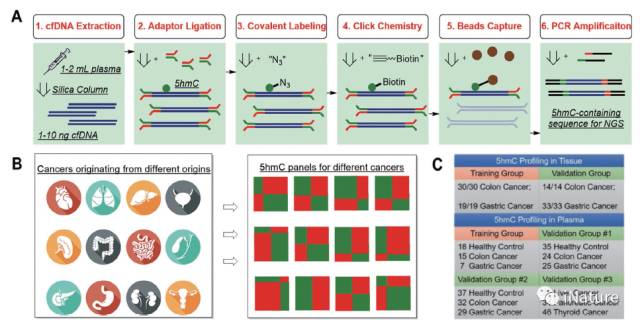
人(rén)类癌症(zhèng)的cfDNA中(zhōng),检测5hmC的生物标(biāo)志物
肿(zhǒng)瘤(liú)相关的(de)cfDNA体细胞突变已经显(xiǎn)示与肿瘤组(zǔ)织共享,尽管低的突(tū)变频率和缺乏来源(yuán)组织(zhī)的(de)信息阻碍了检测的敏感(gǎn)性。 5mC和5hmC来自液体活组织检查(chá)的cfDNA可以(yǐ)作为(wéi)平行(háng)或(huò)更有价值(zhí)的(de)生物标志物(wù),用于人类疾病的非(fēi)侵入(rù)性诊(zhěn)断和预后,因为它们概括(kuò)了相关(guān)细胞状(zhuàng)态(tài)中的基因表达变化。如果(guǒ)可以灵敏地检测这些胞嘧啶修饰模式,则可以鉴定疾(jí)病特异性生物标志(zhì)物,用于早期的肿瘤检测,诊断和预后。
5hmC在癌(ái)细胞的差(chà)异化富集
高(gāo)通量测序是检测(cè)全基因组胞嘧啶修饰模式的理想平台。全基因组亚硫酸氢盐测(cè)序(xù)或替代方法已应(yīng)用于生物标志物研究【26-28】。组织和癌(ái)症特异性甲基(jī)化位点在(zài)跟踪来自循环血(xuè)的(de)来源组织(zhī)中,表现出有希望的(de)潜力。然而,5mC主(zhǔ)要作为人类(lèi)基因组中高背景(jǐng)水(shuǐ)平的抑(yì)制(zhì)性标记,并且其用亚(yà)硫酸氢盐(yán)处理的测序(xù)一直受到广泛的DNA降(jiàng)解。利用(yòng)羟甲基(jī)的存在,选择(zé)性化(huà)学标记可应(yīng)用于使用低(dī)水平的(de)DNA以高(gāo)灵敏度检(jiǎn)测5hmC。在这(zhè)里,何川等研究组(zǔ)建立了5hmC临(lín)床诊断技术,用(yòng)于cfDNA 5hmC分(fèn)析。显示显示cfDNA的5hmC差异富集,是实体瘤的优秀(xiù)标记。
胰腺癌5hmC分布状(zhuàng)况(kuàng)
癌(ái)症cfDNA的动态(tài)在很大程度上(shàng)还不清(qīng)楚。在(zài)简化的(de)模型情况下,肿(zhǒng)瘤组织的gDNA被(bèi)释放到血浆中并且经历降解,达到与来(lái)自正常(cháng)健康(kāng)组织的(de)背景cfDNA类似的平衡。基因座特异性5hmC修饰似乎是(shì)5hmC水平的主要(yào)决定因素,具有(yǒu)组织特异性,然后(hòu)癌症状态增加额(é)外的变化层。这些组织(zhī),以及在较小(xiǎo)的程度上肿(zhǒng)瘤组织释放的DNA中的癌症特(tè)异性信号,略微改变背景血浆cfDNA的5hmC修(xiū)饰谱。从(cóng)肿瘤组织中释放的cfDNA越多,转移越大,给区分(fèn)肿瘤来源的生物学和临床变化提供了更大的能力。因此,整合来自不同组织类型的gDNA的5hmC概(gài)况(kuàng),以实现对癌症生物标志(zhì)物的疾病特异性的未来(lái)评估,将是至关重要的。
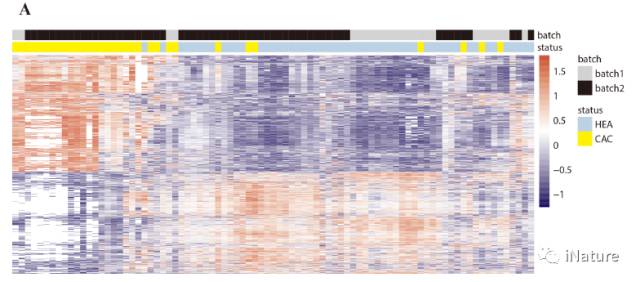
胃癌中(zhōng)5hmC分布状况
此外,实(shí)体瘤由癌干(gàn)细胞(bāo)和(hé)癌细胞组成,在由白细胞,间充质细胞和细(xì)胞(bāo)外基质(zhì)构成的(de)微环境(jìng)中。肿瘤进展启动了以(yǐ)缺氧和血管形(xíng)成(chéng)为特征的局部环境的变化(huà)梯(tī)度。在生长的肿瘤及其周围(wéi)的细胞内(nèi),可能存在广泛的变异性,使得(dé)某些类型的(de)细胞倾向于(yú)凋亡并将DNA释放到(dào)循环(huán)中。
血(xuè)浆cfDNA中观(guān)察到癌症相关5hmC变化(huà)的起源
何川(chuān)等研(yán)究组预计在(zài)血浆cfDNA中观察(chá)到(dào)的5hmC的癌症相关(guān)变化是(shì)由肿(zhǒng)瘤组织内或周(zhōu)围(wéi)的(de)不同组细胞贡献(xiàn)的。肿瘤(liú)相关组织的单细胞(bāo)或细胞类型特(tè)异性5hmC分析和使用适当的细胞(bāo)类型标记(jì)物(wù),将揭示(shì)这些修饰的细胞特异性的(de)程度和分(fèn)布,并进一步阐明有助于(yú)在血浆cfDNA中(zhōng)观察到癌症相关的5hmC变(biàn)化。这是这个(gè)学(xué)科所(suǒ)要达到的意图,同时也是未来的(de)发展(zhǎn)方向(xiàng)。
合肥乐鱼网页版在线登录和中科金臻生(shēng)物医学有限(xiàn)公司 版权所(suǒ)有 皖ICP备16021320号-1 Designed by Wanhu